יחידה 5 – גאומטריה ומבנה מולקולרי
תאוריית VSEPR
Valence Shell Electron Pair Repulsion – דחיית זוגות אלקטרונים בשכבת הוולנס.
העיקרון: זוגות האלקטרונים סביב אטום מרכזי ידחו זה את זה ויתמקמו כמה שיותר רחוק זה מזה.
שלבים
- צייר מבנה לואיס
- ספור את מספר אזורי הצפיפות סביב האטום המרכזי:
- כל קשר (בודד/כפול/משולש) = אזור אחד
- כל זוג בודד = אזור אחד
- קבע את הגאומטריה לפי הטבלה
טבלת הצורות
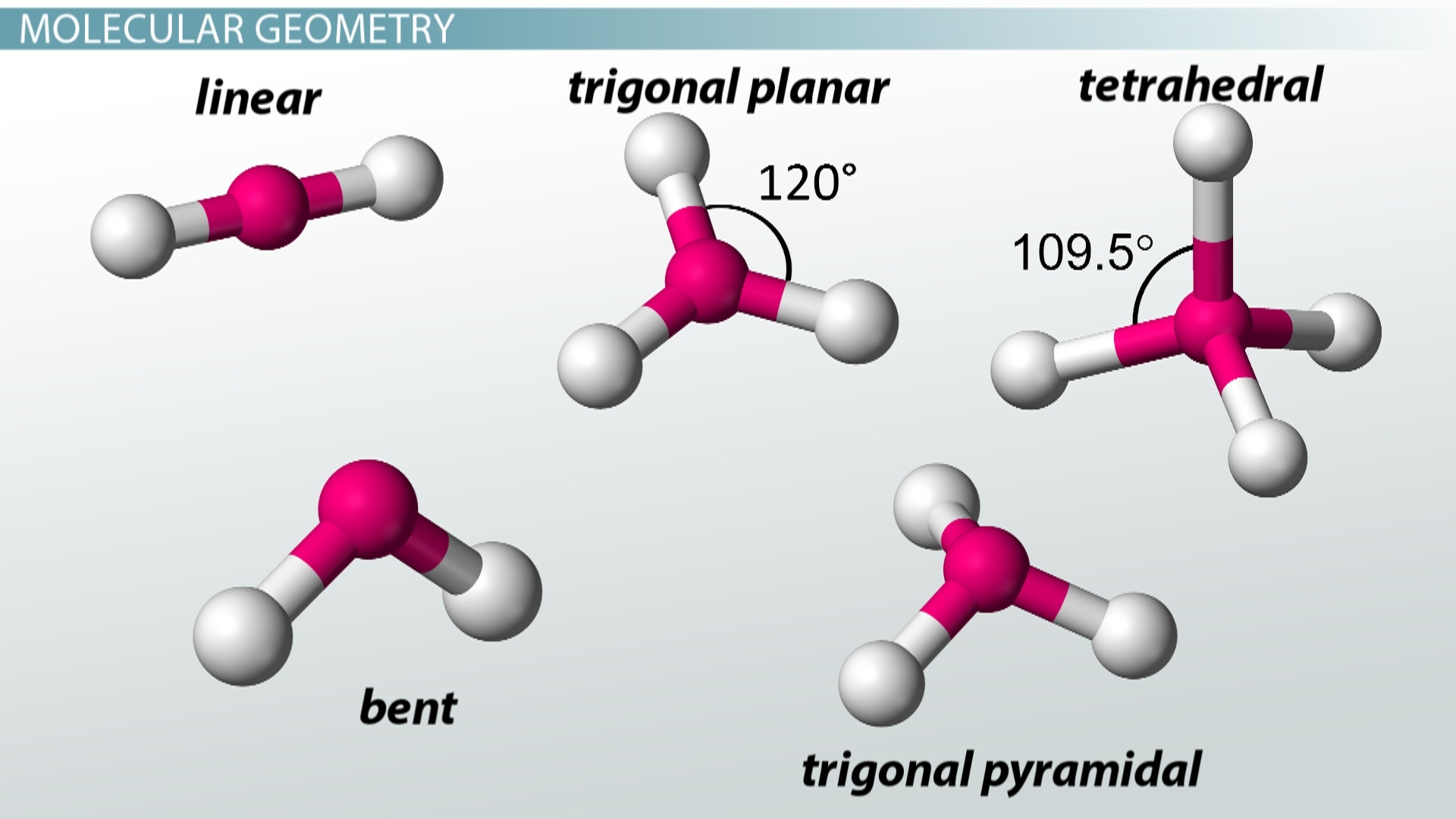
| אזורים | זוגות קושרים | זוגות בודדים | צורה | זווית | דוגמה |
|---|---|---|---|---|---|
| 2 | 2 | 0 | לינארית | , | |
| 3 | 3 | 0 | טריגונלית מישורית | ||
| 3 | 2 | 1 | מכופפת (bent) | ||
| 4 | 4 | 0 | טטראהדרלית | ||
| 4 | 3 | 1 | פירמידה טריגונלית | () | |
| 4 | 2 | 2 | מכופפת (bent) | () | |
| 5 | 5 | 0 | טריגונלית דו-פירמידלית | ||
| 6 | 6 | 0 | אוקטהדרלית |
השפעת זוגות בודדים
זוג בודד תופס יותר מקום מזוג קושר → דוחף את הקשרים → מקטין את הזוויות.
לכן:
קיטוב מולקולרי (פולריות)
מולקולה קוטבית
מולקולה היא קוטבית אם:
- יש קשרים קוטביים () וגם
- הדיפולים לא מתבטלים (אין סימטריה מלאה)
דוגמאות
| מולקולה | קשרים קוטביים? | סימטריה? | פולרית? |
|---|---|---|---|
| כן () | כן (לינארית) | לא – דיפולים מתבטלים | |
| כן () | לא (מכופפת) | כן | |
| קצת () | כן (טטראהדרלית) | לא | |
| כן | לא | כן | |
| כן () | כן (טטראהדרלית) | לא | |
| כן () | לא (פירמידה) | כן |
כלל אצבע: אם כל הליגנדים סביב האטום המרכזי זהים ואין זוגות בודדים → סימטריה → לא קוטבית.
דוגמה טיפוסית למבחן
שאלה: קבעו את הגאומטריה והפולריות של .
פתרון:
- לואיס: עם 3 קשרים ל- וזוג בודד אחד
- אזורי צפיפות:
- צורה: פירמידה טריגונלית (כמו )
- זווית:
- פולריות: קשרים קוטביים + אין סימטריה (זוג בודד) → קוטבית
טעויות נפוצות
| טעות | תיקון |
|---|---|
| "קשר כפול = שני אזורים" | קשר כפול/משולש = אזור צפיפות אחד |
| " קוטבית כי קוטבי" | הדיפולים מתבטלים! לינארית + סימטרית = לא קוטבית |
| "זווית = " | – שני זוגות בודדים דוחפים את הקשרים |
| "4 אזורים = תמיד טטראהדרלי" | רק אם 0 זוגות בודדים! עם 1 = פירמידה, עם 2 = מכופפת |