יחידה 6 – כוחות בין-מולקולריים
סוגי כוחות
חשוב: כוחות בין-מולקולריים (IMF) הם בין מולקולות שונות. לא קשרים כימיים (שהם תוך-מולקולריים).
| כוח | חוזק | בין מי למי | דוגמה |
|---|---|---|---|
| יוני | הכי חזק | יון + יון | (aq) |
| קשר מימן | חזק | קשור ל- ... מול עם זוג בודד | , , |
| דיפול–דיפול | בינוני | מולקולה קוטבית + מולקולה קוטבית | , |
| לונדון (ואן-דר-ואלס) | הכי חלש | כל מולקולה (גם לא קוטבית) | , , |
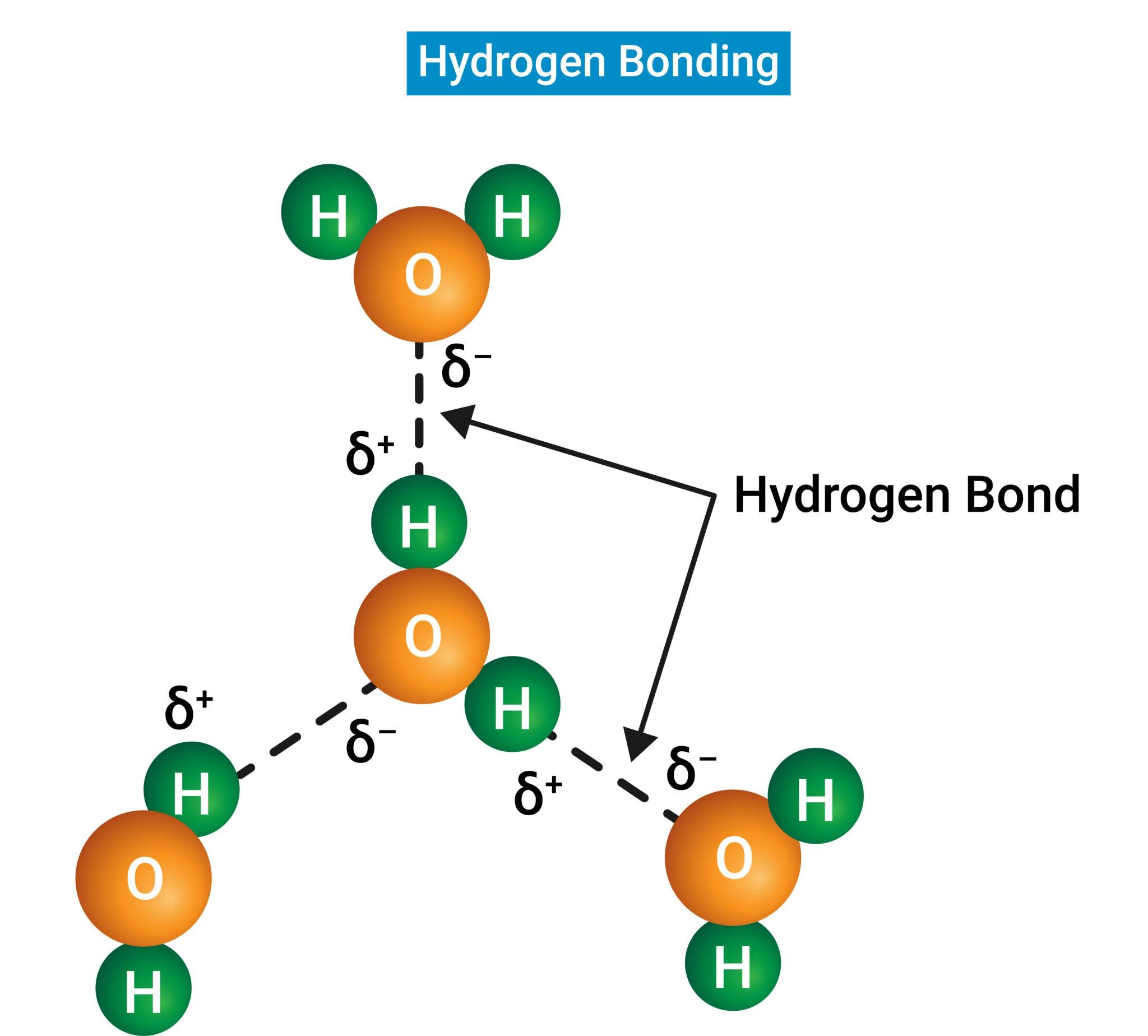
קשרי מימן
תנאים
קשר מימן נוצר כאשר:
- קשור ישירות ל-, , או (אטומים קטנים ואלקטרושליליים מאוד)
- המולקולה השנייה מכילה , , או עם זוג בודד
כאשר .
למה קשרי מימן חזקים יחסית?
- קטן מאוד → הצפיפות החיובית גבוהה
- אלקטרושליליים מאוד → מקטבים חזק את ה-
- הזוג הבודד על נמשך ל- החיובי
דוגמאות
| מולקולה | יש קשרי מימן? | למה? |
|---|---|---|
| כן | ||
| כן | ||
| כן | ||
| לא | לא מספיק אלקטרושלילי | |
| לא | לא | |
| כן | יש ! |
כוחות דיפול–דיפול
בין מולקולות קוטביות – הצד של אחת נמשך לצד של השנייה.
ככל שהדיפול גדול יותר ( גדול יותר) → הכוח חזק יותר.
כוחות לונדון (ואן-דר-ואלס / כוחות פיזור)
קיימים בכל מולקולה – גם לא קוטבית!
מנגנון: תנודות מקריות בענן האלקטרונים יוצרות דיפול רגעי → הוא משרה דיפול במולקולה שכנה → משיכה.
מה משפיע על חוזק לונדון?
| גורם | השפעה |
|---|---|
| גודל/מסה | ככל שהמולקולה גדולה יותר → יותר אלקטרונים → דיפול רגעי חזק יותר |
| שטח פנים | מולקולה מתוחה (שרשרת ארוכה) > מולקולה כדורית (מסועפת) |
דוגמה: -pentane (נקודת רתיחה ) vs neopentane (נקודת רתיחה ) – אותה נוסחה (), אבל ה--pentane ארוך ומתוח → יותר שטח מגע → כוחות לונדון חזקים יותר.
פולריזביליות
מידת הקלות שבה ענן האלקטרונים של אטום/מולקולה מתעוות תחת השפעה חיצונית.
- אטום גדול → ענן רופף → פולריזביליות גבוהה → כוחות לונדון חזקים
- אטום קטן → ענן הדוק → פולריזביליות נמוכה
קשר לנקודת רתיחה
נקודת רתיחה = האנרגיה הנדרשת להפרדת המולקולות זו מזו. ככל שה-IMF חזקים יותר → נקודת רתיחה גבוהה יותר.
סדר ההשפעה
אנומליה של מים
() רותח ב- בעוד () רותח ב-.
למה? יוצר קשרי מימן (חזקים), רק כוחות לונדון ודיפול–דיפול (חלשים).
דוגמה טיפוסית למבחן
שאלה: סדרו לפי נקודת רתיחה עולה: , , , .
פתרון:
| מולקולה | IMF | נ.ר. |
|---|---|---|
| לונדון בלבד (לא קוטבי) | ||
| לונדון (יותר אלקטרונים) | ||
| לונדון + דיפול–דיפול | ||
| לונדון + קשרי מימן |
סדר:
טעויות נפוצות
| טעות | תיקון |
|---|---|
| " יוצר קשרי מימן" | לא! לא מספיק אלקטרושלילי. רק |
| "קשר מימן = קשר כימי" | קשר מימן הוא כוח בין-מולקולרי, לא קשר כימי |
| "מולקולה גדולה = נקודת רתיחה נמוכה" | הפוך! מולקולה גדולה → כוחות לונדון חזקים → נ.ר. גבוהה |
| "לונדון קיים רק במולקולות לא קוטביות" | לונדון קיים בכל מולקולה! |