יחידה 4 – קשרים כימיים
סוגי קשרים
| סוג קשר | בין מי למי | מה קורה | דוגמה |
|---|---|---|---|
| יוני | מתכת + אל-מתכת | העברת אלקטרונים | |
| קוולנטי | אל-מתכת + אל-מתכת | שיתוף אלקטרונים | |
| קוולנטי קוטבי | אל-מתכות עם | שיתוף לא שווה | |
| מתכתי | מתכת + מתכת | "ים אלקטרונים" | , |
מתי יוני ומתי קוולנטי?
| סוג קשר | |
|---|---|
| קוולנטי (לא קוטבי) | |
| קוולנטי קוטבי | |
| יוני |
טעות נפוצה: הגבולות הם מקורבים – אין קו חד. הוא קו מנחה, לא חוק טבע.
מבני לואיס
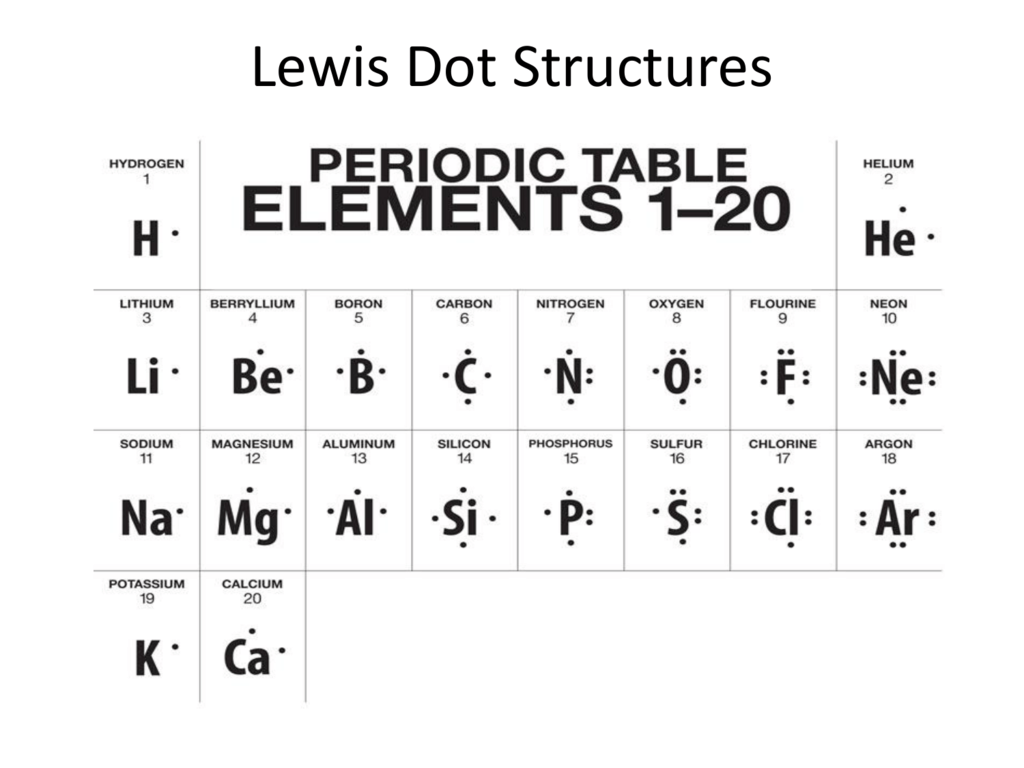
שלבים לבניית מבנה לואיס
- סכמו את אלקטרוני הוולנס של כל האטומים
- חברו את האטומים בקשרים בודדים (כל קשר = 2 אלקטרונים)
- השלימו אוקטטים לאטומים חיצוניים (מסביב)
- בדקו אם לאטום המרכזי יש אוקטט. אם חסר → הפכו זוגות בודדים לקשרים כפולים/משולשים
דוגמה:
- אלקטרוני וולנס: , → סה"כ
- קשרים בודדים: → אלקטרונים
- השלמת אוקטטים ל-O: אלקטרונים נוספים
- ✓ אבל C מקבל רק 4 → צריך קשרים כפולים:
חוק האוקטט וחריגים
רוב האטומים שואפים ל-8 אלקטרונים בשכבת הוולנס.
חריגים
| חריג | דוגמה | הסבר |
|---|---|---|
| פחות מ-8 | ( עם 6), ( עם 4) | אטומים קטנים עם מעט אלקטרונים |
| יותר מ-8 | , | אטומים מהמחזור ה-3+ יכולים להרחיב (יש אורביטלי ) |
| מספר אי-זוגי | (11 אלקטרונים) | רדיקל – אלקטרון בודד |
מטענים פורמליים
| סימן | משמעות |
|---|---|
| אלקטרוני וולנס של האטום (בטבלה) | |
| אלקטרונים בזוגות בודדים (לא קשורים) | |
| אלקטרונים בקשרים |
הכלל: המבנה עם מטענים פורמליים הכי קרובים ל-0 הוא המועדף.
דוגמה:
מטענים פורמליים = 0 לכולם → מבנה מועדף ✓
רזוננס
כשאפשר לכתוב יותר ממבנה לואיס אחד חוקי – המולקולה היא ממוצע (היברידי רזוננס) של כל המבנים.
דוגמה: (אוזון) – שני מבנים שקולים:
בפועל: שני הקשרים שווים באורכם (1.5 בערך).
חשוב: רזוננס ≠ "המולקולה קופצת בין מבנים". המולקולה תמיד במצב הביניים.
טעויות נפוצות
| טעות | תיקון |
|---|---|
| "כל הקשרים יוניים או קוולנטיים" | יש רצף – קשר קוולנטי קוטבי באמצע |
| "H תמיד מרכזי" | לא! H תמיד חיצוני (קשר אחד בלבד) |
| "מטען פורמלי = מטען אמיתי" | מטען פורמלי הוא כלי חישובי, לא מטען פיזיקלי |
| "רזוננס = המולקולה זוגגת" | רזוננס = מצב ביניים קבוע, לא קפיצה |