יונים, גרדיאנטים ופוטנציאל הממברנה
מושגים בסיסיים
| מושג | הסבר |
|---|---|
| יון | אטום או מולקולה בעלי מטען חשמלי כתוצאה מאיבוד או קבלת אלקטרונים |
| קטיון (cation) | יון בעל מטען חיובי (כגון Na⁺, K⁺) |
| אניון (anion) | יון בעל מטען שלילי (כגון Cl⁻) |
| דיפוזיה (diffusion) | תנועה ספונטנית מריכוז גבוה לריכוז נמוך, ללא השקעת אנרגיה |
| כוח חשמלי | משיכה או דחייה הפועלת על יון בהתאם למטענו ולמתח הממברנה |
| שיווי-משקל של יון | מצב שבו אין זרימה נטו של אותו יון דרך הממברנה |
שני הכוחות הפועלים על יונים
על כל יון הפועל בסביבת ממברנה תאית פועלים תמיד שני כוחות:
- הכוח הכימי (גרדיאנט ריכוזים) – תלוי אך ורק בהפרש הריכוזים של היון בין פנים התא לחוץ התא
- הכוח החשמלי – תלוי במטען היון ובמתח החשמלי על פני הממברנה
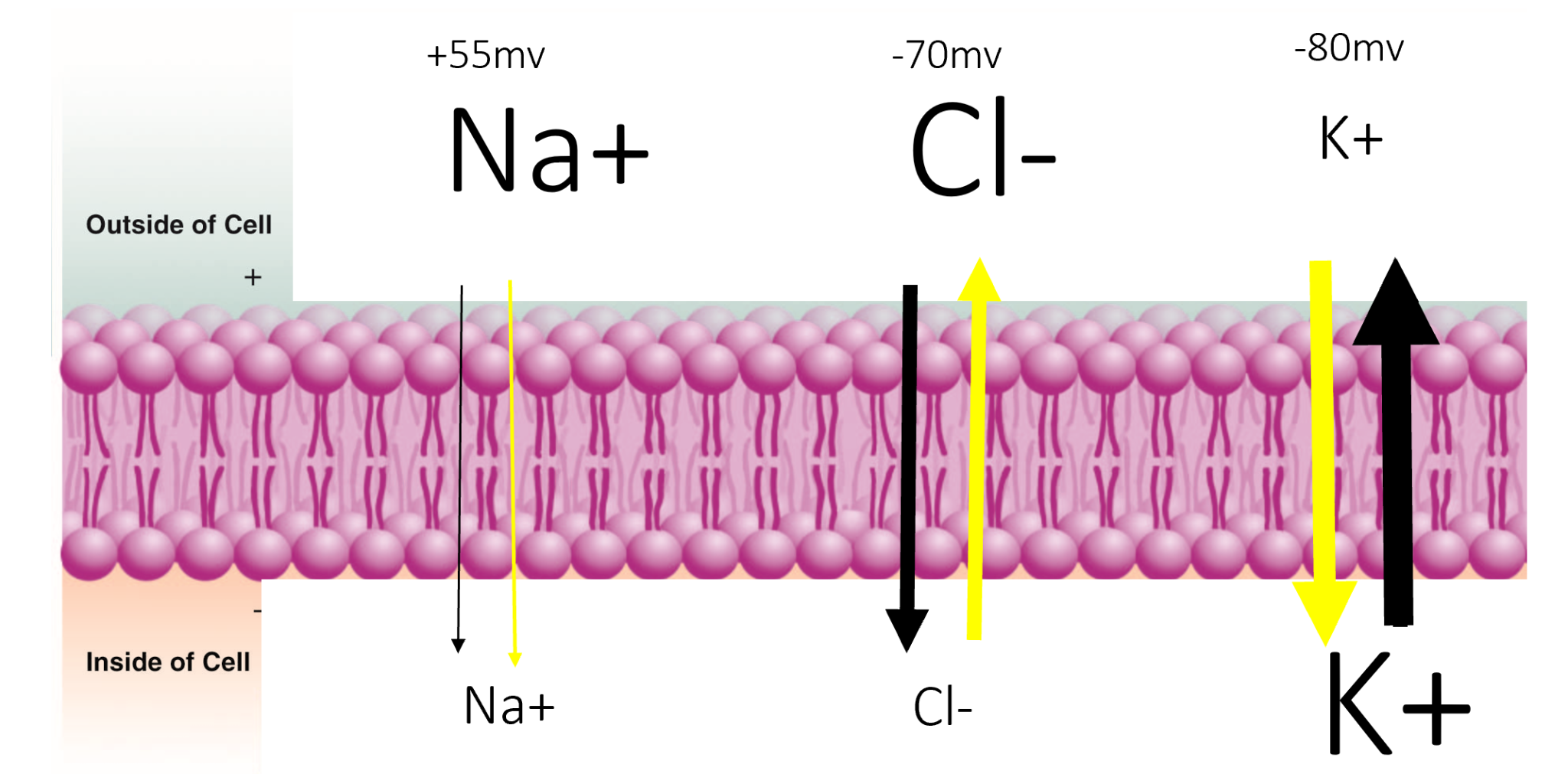
כיוון ועוצמת הזרימה בפועל נקבעים על-ידי השילוב של שני הכוחות יחד, המכונה הגרדיאנט האלקטרוכימי.
הנחה חשובה במצב מנוחה
במצב מנוחה של הנוירון:
כלומר, פנים התא שלילי יחסית לסביבה החוץ-תאית.
מכאן נובע:
- קטיונים נמשכים פנימה ע"י הכוח החשמלי
- אניונים נדחים החוצה ע"י הכוח החשמלי
הרכב יוני כללי - "Salt Water Outside"
הנוזל החוץ-תאי הוא "מלוח" - כמו מי ים!
משמעות הדבר:
- ריכוז Na⁺ ו-Cl⁻ גבוה יותר מחוץ לתא
- ריכוז K⁺ גבוה יותר בתוך התא
הרכב זה הוא הבסיס לגרדיאנטים הכימיים של היונים, ולערכי פוטנציאל שיווי-המשקל שלהם.
טבלת סיכום: ריכוזים, כוחות ו-E_ion
| יון | מטען | ריכוז גבוה | כוח כימי | כוח חשמלי במנוחה | E_ion |
|---|---|---|---|---|---|
| Na⁺ | חיובי | חוץ-תאי | פנימה | פנימה | +55 mV |
| K⁺ | חיובי | תוך-תאי | החוצה | פנימה | -80 mV |
| Cl⁻ | שלילי | חוץ-תאי | פנימה | החוצה | -70 mV |
הגרדיאנט האלקטרוכימי
הגרדיאנט האלקטרוכימי הוא הכוח הכולל הפועל על יון, והוא שילוב של:
- הגרדיאנט הכימי (ריכוזים)
- הגרדיאנט החשמלי (מתח ומטען)
- כאשר שני הכוחות פועלים באותו כיוון → הזרימה חזקה
- כאשר הם פועלים בכיוונים מנוגדים → ייתכן שיווי-משקל
משוואת נרנסט – פוטנציאל שיווי-משקל של יון
משוואת נרנסט מחשבת את פוטנציאל שיווי-המשקל של יון יחיד:
זהו המתח שבו הכוח הכימי והכוח החשמלי מאזנים זה את זה, ולכן אין זרימה נטו של היון.
פירוש הסימנים
| סימן | משמעות |
|---|---|
| פוטנציאל שיווי-המשקל של היון | |
| קבוע הגזים | |
| טמפרטורה מוחלטת | |
| קבוע פאראדיי | |
| מטען היון (+1 ל-Na⁺ ול-K⁺, -1 ל-Cl⁻) | |
| ריכוז היון מחוץ ובתוך התא |
קשר בין נרנסט למתח הממברנה
- אם → אין זרימה נטו של היון
- אם → קיים דחף אלקטרוכימי לזרימה, בתנאי שקיימת תעלה פתוחה
חדירות הממברנה (Permeability)
לא כל היונים חוצים את הממברנה באותה מידה. חדירות מתארת את מספר וסוג התעלות הפתוחות עבור כל יון.
במצב מנוחה:
משמעות:
- קיימות הרבה יותר תעלות פתוחות ל-K⁺
- לכן K⁺ הוא היון הדומיננטי בקביעת פוטנציאל המנוחה
- כתוצאה מכך:
משאבת נתרן-אשלגן (Na⁺/K⁺-ATPase)
משאבת נתרן-אשלגן היא משאבה אקטיבית המשתמשת ב-ATP כדי לשמור על מפלי הריכוזים של Na⁺ ו-K⁺.
בכל מחזור פעולה:
- מוציאה 3 יוני Na⁺ אל מחוץ לתא
- מכניסה 2 יוני K⁺ אל תוך התא
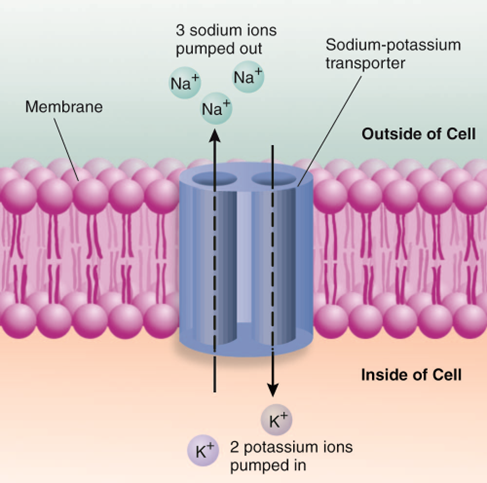
מאפיינים חשובים:
- המשאבה פועלת נגד מפל הריכוזים
- היא אלקטרוגנית – מוציאה יותר מטען חיובי משהיא מכניסה
- תרומתה למתח הממברנה קטנה אך קיימת
תפקידה העיקרי:
- שמירה על מפלי הריכוזים שעליהם מבוססים נרנסט ו-GHK
- אפשרות לקיום מתמשך של פוטנציאלי פעולה
המשאבה אינה יוצרת פוטנציאל פעולה, אלא מאפשרת למערכת החשמלית לפעול לאורך זמן.
יונים ומולקולות שאינם חוצים את הממברנה
הממברנה אינה חדירה ליונים גדולים ולחלבונים טעונים שלילית (A⁻), הכלואים בתוך התא.
חלבונים אלו:
- תורמים לשליליות הפנימית של התא
- משפיעים בעקיפין על פיזור שאר היונים
משוואת Goldman-Hodgkin-Katz (GHK)
משוואת GHK מחשבת את פוטנציאל הממברנה בפועל () כאשר הממברנה חדירה למספר יונים במקביל, וכל יון נשקל לפי החדירות היחסית שלו.
פירוש רכיבי המשוואה
| סימן | משמעות |
|---|---|
| פוטנציאל הממברנה | |
| חדירות הממברנה ליון מסוים | |
| ריכוז היון מחוץ ובתוך התא |
מכיוון ש-Cl⁻ הוא יון שלילי, וכיוון הכוח החשמלי הפועל עליו הפוך.
סיכום למבחן
- נרנסט – יון אחד בלבד
- GHK – כל היונים יחד + חדירות
- פוטנציאל פעולה – שינוי דינמי בזמן של